非酒精性脂肪肝(NAFLD)在全球范围内的患病率为25%,包括一系列肝脏疾病,从简单的脂肪变性到更严重的表现,如肝炎、纤维化、肝硬化,甚至肝细胞癌(Powell等人,2021)。不幸的是,目前还没有有效的药物治疗NAFLD。虽然改变饮食和生活方式可以为预防NAFLD提供一些好处,但在许多国家,普遍实施这些改变仍然具有挑战性。因此,探索膳食补充剂或食用健康食品成为预防NAFLD的潜在替代方案。
当归多糖(ASP)是从当归(Oliv.)Diels中分离得到的主要活性成分,是一种具有保肝作用的强效生物活性化合物。它已在各种肝病模型中证明了疗效,包括脂多糖(LPS)和芽孢杆菌Calmette–Guerin诱导的肝脏免疫损伤、对乙酰氨基酚诱导的急性肝损伤、CCl4诱导的肝纤维化、酒精性脂肪肝(AFLD)(,以及高脂肪饮食(HFD)诱导的NAFLD。大量的体内外实验已经验证了口服多糖的药理潜力(。然而,多糖被小肠中的酶或大肠中的肠道菌群降解为小分子片段。据报道,多糖通过调节肠道菌群的丰度和短链脂肪酸(SCFAs)的水平,在体内发挥多种药理活性(。然而,肠道多糖调节肝脏相关信号通路的确切机制仍不完全清楚。它引起了人们极大兴趣,即在肠道中降解的短链脂肪酸或ASP片段是否会从肠道吸收到肝脏中,从而调节肝脏中的相关信号通路并发挥保肝作用。
线粒体是肝细胞脂肪酸代谢的主要部位。线粒体功能障碍将减少游离脂肪酸(FFAs)的氧化,同时促进活性氧(ROS)的产生。这导致肝脏中的脂质沉积和加重氧化应激,从而加剧NAFLD的发生和进展。据报道,雌激素相关受体α(ERRα)参与线粒体生物发生和自噬的调节,从而缓解NAFLD的进展。研究表明,腺苷5′-单磷酸激活蛋白激酶(AMPK)的磷酸化水平可由丙酸盐调节(Yoshida et al.,2019),通过Esrra启动子激活刺激ERRα转录物的表达。基于这些发现,作者假设ASP在口服后增加肠道丙酸盐水平,从而通过丙酸盐/ERRα途径调节肝细胞线粒体功能,最终缓解NAFLD。
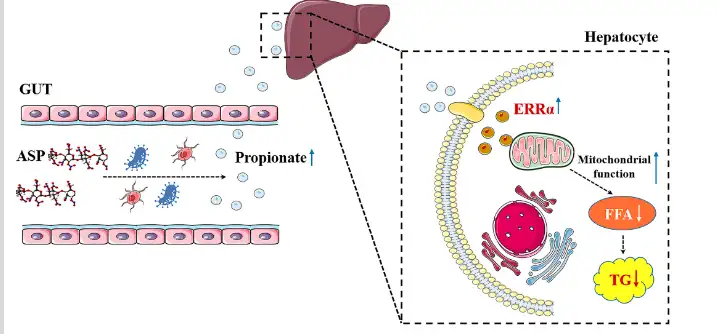
ASP对NAFLD的缓解作用已在之前的研究中得到证实。为了进一步揭示ASP调节肝细胞脂质代谢的根本原因,本研究建立了体内和体外脂质蓄积的NAFLD模型。研究了肠道微生物群的丰度和SCFAs的水平。由于SCFAs水平的变化,在体内和体外研究了丙酸盐/ERRα途径。,ASP被发现可以调节肠道菌群的丰度,并在口服后提高丙酸盐的水平。随后,丙酸盐进入肝脏,通过丙酸盐/ERRα途径调节肝细胞脂质代谢,从而减轻NAFLD。究结果表明,ASP是通过丙酸盐/ERRα途径预防HFD诱导的NAFLD的优秀候选者,这为ASP作为健康护理产品或食品补充剂在持续食用HFD人群中的开发和应用提供了基础。
参考文献:Luo L, Zhang H, Chen W, Zheng Z, He Z, Wang H, Wang K, Zhang Y. Angelica sinensis polysaccharide ameliorates nonalcoholic fatty liver disease via restoring estrogen-related receptor α expression in liver. Phytother Res. 2023 Aug 10. doi: 10.1002/ptr.7982. Epub ahead of print. PMID: 37563852.
版权说明:如非注明,本站文章均为 文译生物-专业的生物医学科研服务专家 原创,转载请注明出处和附带本文链接。